ระบบต่อมไร้ท่อ (Endocrine
system)
ระบบต่อมไร้ท่อทำหน้าที่สัมพันธ์กับระบบประสาทในการควบคุมและประสานการทำงานของร่างกายที่เกี่ยวข้องกับการเจริญเติบโต
เมแทบอลิซึม การสืบพันธ์ รวมถึงการรักษาความสมดุลของน้ำในร่างกาย
เนื่องจากต่อมเหล่านี้ไม่มีท่อ ตัวต่อมจึงหลั่งสารเข้าสู่กระแสโลหิต
สารที่ส่งออกไปเรียกว่า ฮอร์โมน(hormone) จะถูกขนส่งไปสู่อวัยวะทั่วร่างกาย
แต่จะออกฤทธิ์หรือมีผลต่ออวัยวะและเซลล์บางตัวเท่านั้น

ระบบต่อมไร้ท่อในร่างกาย
(2).jpg)



(2).jpg)







ระบบต่อมไร้ท่อในร่างกาย
ระบบต่อมไร้ท่อประกอบด้วยต่อมที่สร้างฮอร์โมน (endocrine
glands) ชนิดต่างๆที่มีขนาดและตำแหน่งที่อยู่แตกต่างกัน ได้แก่ ต่อมไพเนียล (pineal
gland) ไฮโปทาลามัส (hypothalamus)
ต่อมใต้สมอง(pituitary gland) ต่อมไทรอยด์ (thyroid
glands) ต่อมพาราไทรอยด์ (parathyroid glands) ต่อมไทมัส (thymus
gland) ต่อมหมวกไต (adrenals gland) ตับอ่อน (pancreas) และต่อมเพศ (gonads) การทำงานของต่อมเหล่านี้เกิดขึ้นโดยมีฮอร์โมนจากไฮโปทาลามัสทำหน้าที่ควบคุมการหลั่งของฮอร์โมนจากต่อมใต้สมอง
และฮอร์โมนจากต่อมใต้สมองทำหน้าที่ควบคุมการหลั่งฮอร์โมนจากต่อมอื่นๆ ฮอร์โมนเหล่านี้ออกฤทธิ์โดยมีผลกับอวัยวะเป้าหมาย (target
organ) ที่อยู่ข้างเคียง
หรืออวัยวะที่อยู่ห่างไกลโดยปล่อยฮอร์โมนเข้าสู่กระแสโลหิต
ก็สามารถกระจายไปทั่วร่างกาย
ในภาวะปกติฮอร์โมนที่สร้างจากต่อมไร้ท่อจะหลั่งออกมาเป็นช่วงๆ
และอยู่ในกระแสโลหิตช่วงเวลาหนึ่ง ฮอร์โมนแต่ละชนิดจะมีผลต่อเนื้อเยื่อเป้าหมาย (target cell) แตกต่างกันออกไป เช่น ไปกระตุ้น(stimuli)
หรือไปยับยั้ง (inhibit) ความผิดปกติที่เกิดขึ้นของระบบต่อมไร้ท่อมีทั้งภาวะที่ต่อมทำงานมาก (excessive
of hyperfunction) หรือไม่เพียงพอ (insufficiency or
deficiency or hypofunction) ทำให้มีการเปลี่ยนแปลงของระดับฮอร์โมน
เป็นสาเหตุทำให้ต่อมหลั่งฮอร์โมนมาก(hypersecretion)
หรือหลั่งฮอร์โมนน้อย (hyposecretion)
ความผิดปกติของต่อมไร้ท่อ
การทำงานของไฮโปทาลามัสและต่อมพิทูอิทาริมีความสัมพันธ์กันทั้งกายวิภาคและหน้าที่
ความผิดปกติที่ไฮโปทาลามัสจะแสดงออกโดยมีความผิดปกติของการหลั่งฮอร์โมนจากต่อมพิทูอิทาริด้วยเนื่องจากไฮโปทาลามัสเป็นบริเวณที่อยู่ในสมองใกล้กับ
optic chiasm ติดต่อกับต่อมพิทูอิทาริทางpituitary stalk และต่อมพิทูอิทาริเป็นต่อมที่ฐานของสมอง
ตั้งอยู่บนกระดูก sphenoid ที่เป็นแอ่ง เรียกว่า sellaturcicaแบ่งออกเป็น 2 ส่วน คือ ต่อมใต้สมองส่วนหน้า (anterior
pituitary) และต่อมใต้สมองส่วนหลัง (posterior pituitary) ซึ่งถูกควบคุมโดยไฮโปทาลามัส แต่กลไกการควบคุมต่างกัน
ต่อมใต้สมองส่วนหลังมีนิวรอน (neurons) ที่มีจุดเริ่มต้นในไฮโปทาลามัสแต่ต่อมใต้สมองส่วนหน้าไม่มีใยประสาทจากไฮโปทาลามัสมาควบคุมการทำงานของต่อมโดยตรง
แต่จะมีฮอร์โมนจากอวัยวะเป้าหมาย (target organ) เช่น
ต่อมหมวกไต ต่อมไทรอยด์ เป็นต้น มาป้อนกลับ (feed back)
ไฮโปทาลามัส
(hypothalamus)

ไฮโปมาลามัสอยู่บริเวณฐานสมองใหญ่ส่วนหน้าเหนือต่อมใต้สมอง
ทำงานเชื่อมโยงกับต่อมใต้สมองและต่อมไร้ท่ออื่นๆ
ไฮโปทาลามัสสร้างและหลั่งฮอร์โมนได้เอง
เป็นการตอบสนองต่อสัญญาณที่ผ่านมาทางกระแสเลือดหรือเส้นประสาท
เนื่องจากเป็นศูนย์ประสาท (nerve centers) จึงสั่งการเรื่องสำคัญ
เช่น ความกระหาย ความอยากอาหาร อุณหภูมิของร่างกาย และการนอน แบ่ง
hypothalamic hormone ได้เป็น 2 กลุ่ม คือ
1. Posterior pituitary hormone สร้างโดยเซลล์ประสาทในไฮโปทาลามัส ส่งผ่านเส้นประสาท hypothalamo-hypophyseal
nerve ซึ่งทอดยาวไปตาม pituitary stalk ไปเก็บไว้ที่ปลายประสาทซึ่งอยู่ในต่อมใต้สมองส่วนหลัง
ก่อนปล่อยออกสู่กระแสเลือด
2. hypophysiotropic hormone ประกอบด้วย releasing hormone และ inhibiting
hrmoneหลายชนิด หลั่งโดยเซลล์ประสาทของไฮโปทาลามัส
ส่งเข้าหลอดเลือดฝอย และผ่านไปตาม portal vienไปสู่ต่อมใต้สมองส่วนหน้า
ต่อมใต้สมอง
(pituitary
gland หรือ hypophysis)
(2).jpg)
ต่อมใต้สมองมีขนาดเล็กเหมือนเมล็ดถั่วขนาดประมาณ
1cm
หนักประมาณ 500-900 มิลลิกรัม และติดต่อกับ hypothalamus
โดย pituitary stalk ประกอบด้วย 2 ส่วนที่แตกต่างกันทั้งต้นกำเนิด องค์ประกอบ และหน้าที่ ได้แก่
ต่อมใต้สมองส่วนหน้า (anterior pituitary gland or adrenohypophysis) และต่อมใต้สมองส่วนหลัง (posterior pituitary gland or
neurohypophysis) ระหว่างต่อมใต้สมองส่วนหน้าและส่วนหลัง มีส่วนกลาง
(intermediate lobe) ต่อมใต้สมองส่วนกลางของสัตว์เจริญดี
และทำหน้าที่สร้างฮอร์โมน melanophore-stimulating hormone หรือ
melanocyte-stimulating hormone (MSH) แต่ต่อมใต้สมองส่วนกลางในคนเจริญน้อยมาก
ต่อมใต้สมองส่วนหลัง
ต่อมใต้สมองส่วนหลังประกอบด้วยเซลล์ pituicyteและปลายประสาทซึ่งตัวเซลล์อยู่ในไฮโปทาลามัส
เซลล์ประสาทสร้างและหลั่งฮอร์โมน 2 ชนิดคือ ADH (antidiuretic hormone) และ oxytocin ส่งผ่านมาตามใยประสาทซึ่งทอดมาใน pituitary stalk เพื่อเก็บไว้ในรูปแกรนูลที่ปลายประสาทในต่อมใต้สมองส่วนหลัง
และหลอดเลือด inferior hypophyseal artery ซึ่งเลี้ยงต่อมใต้สมองส่วนหลังอยู่นอก
blood-brain barrierดังนั้นฮอร์โมนทั้งสองชนิดจึงหลั่งจากปลายประสาทเข้าสู่หลอดเลือดฝอยบริเวณนี้
และผ่านเข้าสู่ระบบการไหลเวียนเลือดของร่างกายได้
1. ADH (antidiuretic
hormone)
ADH มีหน้าที่ควบคุมดุลน้ำในร่างกาย
ได้แก่ การรักษาปริมาณน้ำในร่างกายและควบคุมออสโมลาลิตีของสารน้ำในร่างกาย มีผลให้ปริมาณปัสสาวะลดน้อยลงและเข้มข้นมากขึ้น
(antidiuretic action หรือ antidiuresis) โดยทำให้มีการดูดซึม free water ที่ distal
nephron น้ำที่ดูดกลับเข้าหลอดเลือดมากขึ้นจะเพิ่มปริมาตรเลือด ทำให้เลือดเข้มข้นน้อยลง
และความดันเลือดเพิ่มสูงขึ้น (vasopressive action) เกิดจาก ADH
ขนาดสูงมีฤทธิ์กระตุ้นเซลล์กล้ามเนื้อเรียบผนังหลอดเลือดแดง
ทำให้หลอดเลือดแดงส่วนปลายตีบจึงมีผลเพิ่มความดันเลือดแดง ในภาวะปกติ ADH มีผลเพียงเล็กน้อยในการควบคุมความดันเลือด แต่มีความสำคัญเมื่อร่างกายเสียเลือดมาก
ในคนที่มี ADH หลั่งปกติจะมีปัสสาวะวันละประมาณ 2 ลิตร ถ้า ADH หยุดหลั่งหรือหลั่งน้อยลง เช่น หลังการดื่มแอลกอฮอล์
(แอลกอฮอล์ไปยับยั้งการหลั่ง ADH) น้ำจะถูกขับออกทางปัสสาวะมากขึ้น
ในทางตรงข้ามถ้า ADH ทำงานเต็มที่ เช่น ในภาวะขาดน้ำหรือมีการเสียเลือด
น้ำถูกดูดกลับมาก ปัสสาวะจึงน้อยลง
ความผิดปกติของการหลั่ง
ADH
- การขาด ADH ทำให้ผู้ป่วยขาดน้ำอย่างรุนแรงจากการเสียน้ำทางปัสสาวะ
ปัสสาวะมากทั้งกลางวันกลางคืน อาจสูงถึงวันละ 20 ลิตร
กระหายน้ำตลอดเวลา ความดันเลือดต่ำ ความเข้มข้นพลาสมาสูง เรียกว่า โรคเบาจืด (diabetes
insipidus, DI) สาเหตุเกิดจากความผิดปกติที่ไฮโปทาลามัสทำให้ไม่มีการหลั่ง
ADH หรือหลั่งได้แต่ถูกขัดขวางไม่ให้ผ่านมายังต่อมสมอง หรือ ADH หลั่งปกติแต่ไตตอบสนองต่อ ADH ได้น้อยหรือไม่ตอบสนอง
- การมี ADH มากผิดปกติ เกิดได้จากหลายสาเหตุ
เช่น ภายหลังการผ่าตัดสมอง การได้รับยาที่มีฤทธิ์กระตุ้น ADH หรือเร่งให้ไตตอบสนองต่อ ADH มากขึ้นเซลล์มะเร็งบางชนิดสร้างสารที่มีฤทธิ์คล้าย
ADH ผู้ป่วยที่มี ADH มากจะมีอาการของการมีน้ำคั่งในร่างกาย
(water retention) ความเข้มข้นของเลือดน้อยลง
โซเดียมในเลือดต่ำกว่าปกติ เซลล์บวมน้ำ ถ้าอาการรุนแรงอาจทำให้เกิดอาการทางสมองได้
2.
oxytocin
oxytocin มีความสำคัญในการ
induction ของ labor โดยทำให้มีการหดตัวของมดลูก
และมีหน้าที่เกี่ยวกับการหดตัว myoepithelial cells ของเต้านมเพื่อช่วยในการหลั่งน้ำนม
ฤทธิ์ที่สำคัญของ oxytocin คือ การกระตุ้นให้มีการหลั่งน้ำนม
(milk ejection หรือ milk letdown) และเพิ่มการหดตัวของกล้ามเนื้อผนังมดลูกขณะคลอดบุตร
estrogen ที่สูงขึ้นในหญิงตั้งครรภ์และระหว่างให้นมบุตรเพิ่มตัวรับ
oxytocin ทำให้เต้านมและมดลูกของหญิงตั้งครรภ์ตอบสนองต่อ oxytocin
ได้ไวขึ้น ตรงข้าม progesterone ยับยั้งการตอบสนองของกล้ามเนื้อผนังมดลูกต่อ
oxytocin ในเพศชาย oxytocin
ไม่แสดงผลใด oxytocin ขนาดสูงมากอาจจับกับตัวรับของ ADH
ทำให้เกิดการคั่งของน้ำในร่างกายได้
ตามปกติระดับ oxytocinในเลือดจะต่ำมาก เมื่อเริ่มต้นการคลอดหรือขณะให้นมบุตร
กระแสประสาทที่ผ่านขึ้นไปตาม spinothalamic tract กระตุ้นเซลล์ของ
PVN ในไฮโปทาลามัส ทำให้ oxytocin หลั่งเพิ่มขึ้น
สัญญาณประสาทที่เพิ่มนี้อาจเนื่องจาก stretch receptor บริเวณปากมดลูกถูกกระตุ้นโดยศีรษะเด็กที่ดันปากมดลูกให้ขยาย
หรือการที่ touch receptor บริเวณหัวนมมารดาถูกกระตุ้นโดยการดูดของทารก
มีผลกระตุ้นให้น้ำนมหลั่งภายใน 30 วินาที สัญญาณจากสมอง เช่น
การได้ยินเสียงร้องของทารกมีผลเพิ่ม oxytocin ทำให้มารดาหลั่งน้ำนมได้
ตรงข้ามความเครียดมีผลยับยั้ง oxytocin ทำให้มารดาไม่มีน้ำนมไหล
โรคที่พบในความผิดปกติของต่อมใต้สมองส่วนหลัง
Diabetes
insipidus (โรคเบาจืด)
โรคเบาจืดเกิดจากมีการหลั่ง ADH (antidiuretic hormone) จำนวนน้อย
ทำให้มีการขับปัสสาวะ มากขึ้น
ความเข้มข้นของเลือดเพิ่มขึ้น กระตุ้นให้ร่างกายกระหายน้ำ (polydipsia) อาการที่พบคือ ปัสสาวะมากและบ่อยครั้งทุก 30-60 นาทีตลอด
24 ชั่วโมง ปริมาณปัสสาวะมากกว่า 3
ลิตรต่อ 24 ชั่วโมง ในรายที่ศูนย์การกระหายน้ำเสีย
ผู้ป่วยไม่รู้สึกตัว การดื่มน้ำจะไม่ทันกับการสูญเสียน้ำออกจากร่างกาย ทำให้อ่อนเพลีย
ปากแห้ง ท้องผูก ไข้ขึ้น อารมณ์ผิดปกติ กระวนกระวาย หมดสติอาจถึงกับเสียชีวิตได้
กลุ่มอาการนี้ต้องแยกจาก solute diuresis เช่น โรคเบาหวาน
และต้องแยกจากการที่มีปัสสาวะบ่อยครั้งแต่ปัสสาวะมีปริมาณและความเข้มข้นที่ปกติ
ต่อมใต้สมองส่วนหน้า
ต่อมใต้สมองส่วนหน้าประกอบด้วยเซลล์สังเคราะห์ฮอร์โมนอย่างน้อย
5 ชนิด ในสัดส่วนที่ไม่เท่ากัน
เซลล์แต่ละชนิดเป็นต้นกำเนิดของฮอร์โมนที่แตกต่างกัน
ฮอร์โมนของต่อมใต้สมองส่วนหน้าอยู่ภายใต้การควบคุมของ releasing และ inhibiting hormone จากไฮโปทาลามัส
มีความสำคัญในการกระตุ้นการหลั่งฮอร์โมนจากต่อมไร้ท่อหลายชนิดในร่างกาย เช่น ต่อมไทรอยด์
ต่อมหมวกไตส่วนเปลือก และต่อมบ่งเพศ (gonad)
รวมทั้งกระตุ้นการเจริญของเซลล์เป้าหมายอื่นๆ จึงเป็น trophic hormone ฮอร์โมนของต่อมใต้สมองส่วนหน้ามีอย่างน้อย 6 ชนิด
ได้แก่ ACTH , TSH, FSH, LH, PRL และ GH ดังนี้
1. ACTH (adrenocorticotrophic
hormone) ออกฤทธิ์ที่ต่อมหมวกไตให้หลั่ง glucocorticoid (cortisol)
ซึ่งมีผลต่อการสลายไขมันเพื่อที่ร่างกายจะนำไปใช้ในกรณีอดอาหาร ลดน้ำหนัก
และยังช่วยพากลูโคสเข้าสู่เซลล์ และ ACTHยังกระตุ้น MSH
(melanocyte stimulating hormone)
ซึ่งมีผลต่อสีของผิวหนังที่คล้ำขึ้น ในปัจจุบันพบว่า ผิวหนังเป็นแหล่งสร้าง ACTH ด้วย มีผลต่อเซลล์ของสีผิว รากขน และระบบภูมิคุ้มกันที่ผิวหนัง
ซึ่งอาจเป็นสาเหตุของโรคผิวหนังบางชนิด
และอาการแพ้หรือการอักเสบจากผิวหนังที่พบเนื่องจากภาวะเครียด และความเครียด
การติดเชื้อ ไข้สูง ภาวะน้ำตาลในเลือดต่ำ (hypoglycemia)
ก็เป็นปัจจัยที่มีผลต่อการกระตุ้นทำให้การหลั่ง ACTH มากกว่าปกติ
ส่งผลทำให้เกิดโรคCushing syndrome
2. TSH (thyroid stimulating hormone) ออกฤทธิ์ที่ต่อมไทรอยด์ทำให้มีการสังเคราะห์และหลั่ง
thyroid hormone เพิ่มขึ้น (T3=triodotyronine,
T4=tetraiodotyronine) ซึ่งควบคุมเมแทบอลิซึมของร่างกาย
ค่าปกติของระดับ TSH เท่ากับ 0.5-5 microunit/mlถ้ามีการหลั่ง thyroid hormone มากกว่าปกติเรียกว่า hyperthyroidism
ถ้ามี thyroid hormone ปริมาณน้อยเรียกว่า hypothyroidism
3. FSH (follicular stimulating hormone) ออกฤทธิ์ที่ต่อมเพศ
(gonads) มีหน้าที่ในการควบคุมการเติบโตของ testis และ gametogenesis ในเพศหญิง มีผลทำให้ follicle
ในรังไข่ (ovary) เจริญเติบโตขึ้น
และการหลั่งฮอร์โมนเอสโตเจน (estrogen) ซึ่งมีผลต่อการเจริญของเยื่อบุโพรงมดลูกและเต้านม
ในเพศชาย FSH ออกฤทธิ์ผ่าน sertoli cell ทำให้เกิดการสร้างเชื้ออสุจิ (spermatogenesis)
4. LH (luteinizing hormone) ออกฤทธิ์ที่ต่อมเพศ
ในเพศหญิง LH จะกระตุ้นให้ไข่ที่สุกเต็มที่แล้วเกิดการตกไข่
เรียกว่า ovulation และเกิด luteinizationของ ovarian follicle และมีผลต่อ interstitial
cellsทำให้สร้าง estrogen และ progesterone
มีผลต่อเยื่อบุโพรงมดลูกและเต้านม ถ้าไข่ไม่ได้ถูกผสมฮอร์โมนเอสโตรเจนและโปรเจสเตอโรนจะลดลง
เกิดการสลายตัวและหลุดลอกของเยื่อบุผนังมดลูกเกิดเป็นเลือดประจำเดือน ในเพศชาย LH
ทำให้ interstitial cells สร้าง testosterone
ซึ่งเกี่ยวข้องกับการเจริญเติบโตของอวัยวะเพศ
5. PRL (prolactin) มีผลต่อการกระตุ้นต่อมน้ำนม
(mammary gland) ในการสร้างน้ำนมของเพศหญิง
ฮอร์โมนนี้จะมีปริมาณสูงขึ้นมากในผู้หญิงใกล้คลอดและหลังคลอดใหม่ๆ ถ้ามี PRL
สูงมากๆจะมีผลช่วยลดการหลั่ง GnRHทำให้ประจำเดือนผิดปกติไปหรือไม่มีประจำเดือน
ดังนั้นการแนะนำให้มารดาเลี้ยงทารกด้วยนมมารดาจะช่วยคุมกำเนิดโดยวิธีธรรมชาติ
เมื่อทารกหย่านมมารดารอบประจำเดือนจะกลับคืนมา และสามารถตั้งครรภ์ได้ใน 4-5
สัปดาห์ ส่วนในเพศชายยังไม่ทราบหน้าที่แน่นอน แต่ถ้ามีปริมาณ PRL มากกว่าปกติในผู้ชายจะมีนมโตขึ้นเรียกว่าgynecomastia
6. GH (growth hormone)
เป็นฮอร์โมนที่สำคัญเกี่ยวกับการเจริญเติบโตและเมแทบอลิซึมของร่างกาย จะสูงสุดเมื่อเข้าสู่วัยรุ่นและลดลงภายหลังอายุ
20 ปี ในแต่ละวัน GH จะหลั่งสูงสุดหลังหลับสนิทประมาณ
1-1.30 ชั่วโมง ผลที่เกิดจาก GH ในร่างกายมี
2 ชนิดคือ
- ผลโดยตรง เกิดจากการที่ GH จับกับตัวรับเซลล์เป้าหมาย เช่น เซลล์ป้าหมายเป็นเซลล์ไขมัน
เซลล์ไขมันจะมีตัวรับ GH จะกระตุ้นให้เกิดการสลายไขมันชนิดไตรกลีเซอไรด์
และยับยั้งการสะสมไขมันที่ล่องลอยอยู่ในกระแสเลือด
- ผลโดยอ้อม GH จะออกฤทธิ์ผ่านโซมาโทมีดิน (somatomedin)
กระตุ้นให้มีการสร้างIGF-1 จะไปออกฤทธิ์ที่อวัยวะเป้าหมายอีกทีหนึ่ง
บทบาทของ IGF-1
- กระตุ้นการแบ่งตัวของเซลล์สร้างกระดูกอ่อน
ทำให้เกิดการเจริญเติบโตของกระดูก
- กระตุ้นให้มีการเจริญเติบโตของกล้ามเนื้อ
โดยกระตุ้นเซลล์ไมโอบลาสท์ให้แบ่งตัวเพื่อทำหน้าที่เฉพาะเจาะจงและเพิ่มจำนวนเซลล์
และกระตุ้นการนำกรดอะมิโนมาใช้
รวมทั้งกระตุ้นการสังเคราะห์โปรตีนในกล้ามเนื้อและเนื้อเยื่ออื่นๆ
ผลของ GH
ที่มีต่อกระบวนการเมแทบอลิซึม
- ผลต่อโปรตีน กระตุ้นการสังเคราะห์โปรตีน
ลดปฏิกิริยาการเผาผลาญโปรตีน และสามารถนำกรดอะมิโนมาใช้มากขึ้น
โดยรวมถือว่าเป็นการเพิ่มเมแทบอลิซึมของโปรตีนในร่างกาย
ผู้สูงอายุที่มีมวลกล้ามเนื้อลดลงส่วนหนึ่งเนื่องมาจากการหลั่ง GH
ลดลง
- ผลต่อไขมัน GH
มีฤทธิ์เพิ่มการใช้ไขมัน กระตุ้นการสลายตัวของไตรกลีเซอไรด์
และช่วยเร่งปฏิกิริยาภายในเซลล์ไขมันชนิดอะดิโปซัยท์
- ผลต่อคาร์โบไอเดรต GH ช่วยควบคุมระดับน้ำตาลในเลือดให้อยู่ในเกณฑ์ปกติ โดยออกฤทธิ์ตรงข้ามกับฮอร์โมนอินซูลิน
ตัวของมันเองยับยั้งฤทธิ์ของอินซูลินที่เนื้อเยื่อปลายทาง
และยังกระตุ้นให้ตับสร้างกลูโคสออกมามากขึ้น
- GH เร่งไตให้ดูดกลับฟอสฟอรัส
(PO4)ได้มากขึ้น
ในขณะที่ทางเดินอาหารดูดซึมแคลเซียม (Ca3)ได้ดีขึ้น อาจเนื่องจาก GH
กระตุ้นการสังเคราะห์วิตามินดี ผลรวมคือมี Ca3(PO4)2มากขึ้นสำหรับการสร้างกระดูก
ระดับปกติของ
GH มีค่าเท่ากับ 3-5 nanogram/ml ถ้าปริมาณของ GHสูงมากกว่าปกติในวัยเด็กเรียกว่า gigantism สำหรับผู้ใหญ่เรียกว่า
acromegaly แต่ถ้าปริมาณ GH หลั่งออกมาน้อยในเด็กเรียกว่า
dwarfism ในทางคลินิกการวัดระดับ IGF-1
ในเลือด ช่วยการวินิจฉัยแยกคนปกติ acromegaly และ
dwarfism ออกจากกันได้
ความผิดปกติของการหลั่ง GH
- GH หลั่งน้อยผิดปกติ เด็กขาด
GH จะตัวเตี้ย (dwarfism) โดยสัดส่วนร่างกายและสติปัญญาไม่ผิดปกติ
สาเหตุที่ขาด GH อาจเนื่องจากความผิดปกติที่เซลล์สังเคราะห์ GHRH
หรือที่ somatotrophหรือส่วนของตัวรับ GH
ผิดปกติ ทำให้ GH ออกฤทธิ์ไม่ได้
ตับไม่สามารถสร้าง IGF-1 ผู้ใหญ่ที่เติบโตเต็มที่ถ้าขาด GH
พบมีไขมันสะสมมากขึ้น โปรตีนลดลง กล้ามเนื้อและกระดูกอ่อนแอ
ผิวหนังบาง เกิดภาวะน้ำตาลในเลือดต่ำง่าย
- GH หลั่งมากผิดปกติ
สาเหตุมักเกิดจากเนื้องอกของ somatotrophในต่อมใต้สมอง
เด็กที่ epiphysis ยังไม่ปิด ถ้ามี GH
มากผิดปกติ จะมีส่วนสูงมากเมื่อเทียบกับเด็กปกติอายุเท่ากัน อาจสูงถึง 2.5 เมตร(gigantism) อย่างไรก็ตามเนื่องจาก GH เร่ง epiphysis ให้ปิดด้วย
ความสูงเมื่อเป็นผู้ใหญ่ในบางรายจึงอาจไม่ผิดปกติชัดเจน
อาจพบมีโรคเบาหวานหรือโรคหัวใจร่วมด้วย
ผู้ใหญ่ที่ epiphysis ปิดแล้ว ถ้ามี GH มาก พบว่ากระดูกที่เป็น membranous
bone เช่น กะโหลกศีรษะ ขากรรไกร มือเท้า จะเจริญมากผิดปกติ (acromegaly) แต่ไม่สามารถสูงเพิ่มขึ้นได้อีก
อวัยวะภายในและเนื้อเยื่อต่างๆเจริญมากผิดปกติ เสียงห้าวลึก gigantism ที่ไม่ได้รับการรักษาก่อนเข้าสู่วัยรุ่นอาจเกิด acromegaly ร่วมด้วยได้
โรคที่พบในความผิดปกติของต่อมใต้สมองส่วนหน้า
สาเหตุความผิดปกติของการหลั่งฮอร์โมนจากต่อมใต้สมองมีหลายอย่าง
เช่น ความผิดปกติแต่กำเนิด ความผิดปกติของระบบภูมิคุ้มกัน การได้รับอุบัติเหตุ
และเนื้องอกหรือมะเร็งจากต่อมไร้ท่อ
ความผิดปกติของต่อมใต้สมองทำงานมากกว่าปกติ (hyperpituitarism) ที่พบบ่อยคือ เนื้องอกของ
ต่อมใต้สมอง (pituitary adenoma)
ส่วนความผิดปกติของต่อมใต้สมองทำงานน้อย (hypopituitarism)
แบ่งออกเป็น 2 ชนิดคือ primary hypopituitarism เกิดจากต่อมใต้สมองฝ่อเหี่ยวไป และ secondary hypopituitarism เกิดจากไฮโปทาลามัสผิดปกติ หลั่งฮอร์โมนชนิด hypothalamic hormone น้อย
Dwarfism

โรค Dwarfism
เกิดจากการขาด GH และ epiphyseal plate ปิดก่อนเป็นโรค Dwarfism เด็กที่ขาด GH จะมีหน้าตาที่ดูอ่อนกว่าอายุจริง รูปร่างเตี้ยเล็กแต่สมส่วน
อ้วนกลมเนื่องจากมีไขมันสะสมบริเวณลำตัวมาก น้ำตาลในเลือดต่ำ
ถ้าเป็นเด็กชายมักมีอวัยวะเพศเล็กไม่สมวัย การขาด GH ไม่มีผลกระทบต่อระดับสติปัญญาของเด็ก
(แต่มักมีปัญหาด้านจิตใจ) ร่างกายเตี้ยแคระไมได้เกิดจากการขาด GH เสมอไป บางครั้ง GH ในกระแสเลือดปกติ
แต่ตัวรับสัญญาณไม่ตอบสนองต่อ GH มักอาจเกิดจากการผ่าเหล่า (mutation) ของยีนของตัวรับสัญญาณทำให้ GH ทำงานไม่ได้
เรียกการเตี้ยแคระแบบนี้ว่า เตี้ยแคระแบบลาร์สันหรือการไม่ตอบสนองต่อ GH (Larsondwarfism หรือ growth hormone
insensitivity)
นอกจากการขาด GH
แล้ว การขาดไทรอยด์ฮอร์โมนละฮอร์โมนเพศยังมีผลทำให้เด็กเตี้ย
แต่การขาดไทรอยด์ออร์โมนมักมีผลทางด้านสติปัญญาร่วมด้วย
การมีฮอร์โมนจากต่อมหมวกไตมากเกินไปก็ทำให้เด็กมีรูปร่างอ้วนเตี้ยได้
Gigantism

โรค Gigantism เกิดจากการมี GH สูงมาก
พบในวัยรุ่นไม่ค่อยพบในวัยเด็ก อาจเกิดจากการมี เนื้องอกของเซลล์ที่สร้างฮอร์โมน (somatotrop) หรือของไฮโปทาลามัส เมื่อร่างกายมีการผลิต GH มากเกินไปก็ทำให้ร่างกายใหญ่โต
โดยผู้ป่วยส่วนมากจะมีความสูงเกิน 200 เซนติเมตร
มีการเจริญของกระดูกไปตามยาว
แขนขายาวเร็วมากจนเป็นร่างยักษ์เนื่องจากส่วนของกระดูก epiphyseal plate ยังไม่ปิด
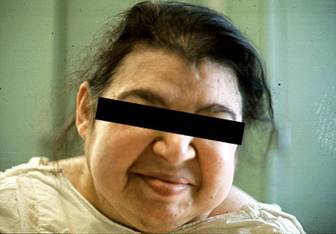
Acromegaly

โรค Acromegaly เป็นโรคที่เกิดจากการมี
GH สูงมากในวัยผู้ใหญ่ ซึ่งวัยนี้ปลายกระดูกปิดแล้ว (epiphyseal
plate) ทำให้มีการขยายตัวของกระดูกอ่อนที่ยังปรากฏอยู่ เช่น
กระดูกบริเวณใบหน้ายาวทำให้มีใบหน้ายาว จมูกและ frontal bone มีขนาดใหญ่ขึ้น คางใหญ่และยื่นออก ฟันล่างสบกับฟันบนผิดปกติ ฟันห่างออก
ลิ้นใหญ่ สายเสียงหนาตัวขึ้น ทำให้มีเสียงห้าวและต่ำ มือเท้ามีขนาดใหญ่
ต่อมไขมันและต่อมเหงื่อโตขึ้น ทำให้เหงื่ออกมาก อวัยวะภายในใหญ่ขึ้น เช่น ตับ ไต
ม้าม ต่อมไทรอยด์ ต่อมหมวกไต หัวใจ
ข้อขยายขึ้นทำให้ปวดข้อ มีน้ำตาลในเลือดสูงขึ้นเป็นเบาหวานได้
สภาพโตเกินไม่สมส่วนหรืออะโครเมกาลี (Acromegaly) เป็นกลุ่มอาการที่เกิดขึ้นเมื่อต่อมใต้สมองทำงานผิดปกติ สร้าง GH
มากกว่าปกติ หลังจากที่ epiphyseal plate ปิดลงแล้ว
โรคนี้มีการดำเนินโรคแบบค่อยเป็นค่อยไป
ใช้เวลาหลายปีหรือหลายสิบปีกว่าอาการจะปรากฏให้เห็นชัด
อายุโดยเฉลี่ยเมื่อได้รับการวินิจฉัยอยู่ที่ 40-45 ปี
ต่อมไทรอยด์ (thyroid gland)
(2).jpg)
ไทรอยด์วางอยู่บนหลอดลมมีสอง lobe ทำหน้าที่สังเคราะห์ฮอร์โมน สารต้นกำเนิดไทรอยด์ฮอร์โมนคือ กรดอะมิโน tyrosine
และ iodine โดย iodine ในอาหารถูกเปลี่ยนเป็น
iodide ก่อนถูกดูดซึมที่ลำไส้เข้ากระแสเลือด ตามปกติในแต่ละวันประมาณร้อยละ
20 ของ iodide ที่ได้รับจากอาหารถูกจับเข้า ต่อมไทรอยด์ แต่ถ้าร่างกายขาด iodine ต่อมจะจับเพิ่มขึ้นเป็นร้อยละ 80-90 ไทรอยด์ฮอร์โมนมี
2 ชนิด ได้แก่ thyroxineหรือ tetraiodothyronine(T4) และ triodothyronine(T3)
Thyroid autoregulationเป็นกลไกที่ต่อมไทรอยด์พยายามรักษาปริมาณการสร้างไทรอยด์ฮอร์โมนให้คงที่
เนื่องจากปริมาณ iodine ในอาหารมักเปลี่ยนแปลงตลอดเวลา
ดังนั้นเพื่อไม่ให้ขาดไทรอยด์ฮอร์โมนในภาวะที่ร่างกายขาด iodine ต่อมจะรับ iodine เข้ามากขึ้น และตอบสนองต่อ TSH
ได้ดีขึ้น ตรงข้ามถ้าในเลือดมี iodine มาก
ต่อมจะรับ iodine เข้าน้อยลง และตอบสนองต่อ TSH ลดลง
ปัจจัยที่มีอิทธิพลต่อการสร้างและการหลั่งฮอร์โมนของต่อมไทรอยด์
ได้แก่ TSH
จากต่อมใต้สมอง และ TRH จากไฮโปทาลามัส
การป้อนกลับเชิงลบของไทรอยด์ฮอร์โมนในเลือดต่อ TSH และ TRH
รวมทั้ง thyroid autoregulation
TRH (thyrotropin-releasing
hormone) เป็นโปรตีนถูกสร้างและหลั่งโดยเซลล์ไฮโปทาลามัสออกฤทธิ์ผ่านตัวรับบนเยื่อหุ้มเซลล์
thyrotrophในต่อมใต้สมองส่วนหน้า กระตุ้นให้สร้างและหลั่ง TSH
เพิ่มขึ้น และเพิ่มการหลั่ง prolactin ด้วย
อุณหภูมิกายที่ลดลงมีผลกระตุ้น TRHcortisol ที่สูงขึ้นยับยั้ง
TRH
TSH (thyrotropinหรือ thyroid stimulating hormone) ออกฤทธิ์ผ่านตัวรับที่เยื่อหุ้มเซลล์ต่อมไทรอยด์
เพิ่มปริมาณเลือดที่เลี้ยงต่อมไทรอยด์
กระตุ้นให้เซลล์ของฟอลลิเคิลเจริญขยายขนาดและเพิ่มจำนวนมากขึ้น TSH ที่เพิ่มสูงขึ้นเป็นเวลานานมีผลให้ต่อมไทรอยด์เจริญขยายขนาดขึ้นเรื่อยๆเรียก
goiter
นอกจาก TRH แล้ว ปัจจัยอื่น เช่น อากาศที่หนาวจัด ฮอร์โมนเพศหญิง(estrogen) ยาที่มีฤทธิ์เหมือน catecholamine กระตุ้น TSH
ให้หลั่งเพิ่มขึ้น ตรงข้าม thyroid hormone, cortisol ขนาดสูง, dopamine, somatostatin, GH และtestosterone
ยับยั้งการหลั่ง TSH
กลไกการป้อนกลับของ T4
และ T3 ต่อ TSH และ TRH
ช่วยรักษาระดับ Free T4 และ Free T3 ในเลือดให้คงที่ การเปลี่ยนแปลงระดับT4 และ T3
ในเลือดเพียงร้อยละ 10-30 มีผลให้ระดับ TSH
เปลี่ยนไปในทางตรงข้าม
ฤทธิ์ของไทรอยด์ฮอร์โมนที่สำคัญได้แก่
การควบคุมเมแทบอลิซึมของร่างกายและจำเป็นสำหรับการเจริญเติบโตและพัฒนาการของร่างกายให้เป็นไปอย่างปกติ
ไทรอยด์ฮอร์โมนเพิ่มการสร้างความร้อนในร่างกายทำให้อัตราเมแทบอลิซึมพื้นฐาน (BMR) เพิ่มสูง อุณหภูมิกายสูงขึ้น
เกิดการปรับตัวเพื่อลดความร้อนในร่างกายโดยการเพิ่มการขับเหงื่อ
การหายใจและการไหลเวียนเลือด
ไทรอยด์ฮอร์โมนกระตุ้นเซลล์กล้ามเนื้อหัวใจทำให้หัวใจเต้นแรงและเร็วขึ้น
ปริมาณเลือดไปเลี้ยงเซลล์มากขึ้น เซลล์ได้รับออกซิเจนมากขึ้นตามมา และยังเร่งการดูดซึมกลูโคสจากทางเดินอาหารและกระบวนการสลายไกลโคเจนในตับ
เซลล์จะมีกลูโคสเพื่อใช้เป็นพลังงานเพิ่มขึ้น ผลโดยรวมจึงทำให้ร่างกายสามารถดึงพลังงานสะสมออกมาใช้ได้มากขึ้นเมื่อจำเป็น
ถ้ามีไทรอยด์ฮอร์โมนมากเมแทบอลิซึมจะสูง น้ำหนักตัวลด ตรงข้ามการขาดไทรอยด์ฮอร์โมนมีผลให้เมแทบอลิซึมลดลง
น้ำหนักตัวเพิ่มขึ้น
นอกจากผลต่อเมแทบอลิซึมของร่างกายที่มีผลต่อการเจริญเติบโตแล้ว
ไทรอยด์ฮอร์โมนยังมีความสำคัญต่อการเจริญสมบูรณ์ของกระดูก ในเด็กที่ขาดไทรอยด์ฮอร์โมนแต่กำเนิดจะเจริญช้า
ฟันขึ้นช้า ตัวเตี้ย (dwarfism) ไทรอยด์ฮอร์โมนเร่งการสร้างและการหลั่ง GH กับ IGF
และร่วมกันทำให้ร่างกายเจริญเติบโต การขาดไทรอยด์ออร์โมนมีผลให้ GH
กับ IGF หลั่งน้อยลงด้วย
ถ้ามีไทรอยด์ฮอร์โมนมากผิดปกติ การสลายกระดูกจะรวดเร็วขึ้นพร้อมกับการสร้างกระดูก
ผลรวมคือมวลกระดูกกลับลดลง
การเจริญ พัฒนาการและการทำงานของเซลล์สมอง
และเซลล์ประสาทต้องอาศัยไทรอยด์ฮอร์โมน โดยเฉพาะระยะเป็นทารกในครรภ์จนถึง 2
ปีหลังคลอด ซึ่งเป็นระยะสำคัญที่สุด เด็กที่ขาดไทรอยด์ฮอร์โมนแต่กำเนิดมีความผิดปกติของเซลล์สมองและประสาท
ถ้าไม่ได้รับไทรอยด์ทดแทนภายใน 1
เดือนหลังคลอดอาจเกิดความพิการอย่างถาวรของสมองและประสาท ปัญญาอ่อน (mental
retardation)
นิยมตรวจหาภาวะไทรอยด์ฮอร์โมนบกพร่องแต่กำเนิดในทารกแรกคลอดทุกราย
เด็กโตและผู้ใหญ่ที่ขาดไทรอยด์ฮอร์โมนมักไม่ค่อยตื่นตัว กระบวนการคิด
การเกิดอารมณ์ และการตอบสนองต่อตัวกระตุ้นทางระบบประสาทช้า
ความจำและความสนใจในการเรียนรู้เสียไป
ความผิดปกติเหล่านี้จะหายไปถ้าได้รับไทรอยด์ฮอร์โมนทดแทน
ตรงข้ามผู้ที่มีไทรอยด์ฮอร์โมนมากผิดปกติมักตื่นตัวง่าย ไม่อยู่นิ่ง สมาธิเสีย
และนอนไม่หลับ
ภาวะขาดไทรอยด์ฮอร์โมนทำให้เกิดการสะสมของ
glycosaminoglycan ใต้ผิวหนัง เกิดการบวมชนิดกดไม่บุ๋ม (myxedema) โดยเฉพาะที่ใบหน้าและรอบตา ลิ้นโตคับปาก และเสียงแหบ
โรคที่พบในความผิดปกติของต่อมไทรอยด์
Hyperthyroidism
Hyperthyroidism เกิดจากการเพิ่มระดับของ
T3 และ T4 ในกระแสเลือด
โดยส่วนใหญ่จะเกิดจากการทำงานเพิ่มมากเกินปกติของต่อมไทรอยด์จึงมักเรียกว่า Hyperthyroidism หรือมาจากสาเหตุอื่นนอกจากต่อมไทรอยด์ จึงอาจพูดได้ว่า Hyperthyroidism เป็นเพียงสาเหตุหนึ่งของ thyrotoxicosis บางครั้งจะใช้คำว่า
primary hyperthyroidism แทนโรคที่มีสาเหตุจากความผิดปกติในต่อมไทรอยด์เอง
ส่วน secondary
hyperthyroidism เป็นกระบวนการนอกต่อมไทรอยด์มักใช้คำว่า thyrotoxicosis แทนกันกับ hyperthyroidism
ระดับของ thyroid hormone ที่เพิ่มขึ้นทำให้มีการเพิ่ม basal metabolic rate ผิวหนังผู้ป่วยจะนุ่ม
อุ่นและแดง เนื่องจากมีการเพิ่มขึ้นของเลือดที่ไปเลี้ยง
ผู้ป่วยจะมีเหงื่ออกมากขึ้นเนื่องจากมีระดับ calorigenesisมากขึ้น
น้ำหนักลดแม้ว่าจะรับประทานได้มากขึ้น
อาการทางหัวใจเป็นอาการที่พบได้เร็วที่สุดและเป็นอาการที่พบได้เสมอในผู้ป่วย hyperthyroidism ผู้ป่วยจะมีอาการหัวใจเต้นเร็ว ใจสั่นและหัวใจโต มักพบ หัวใจเต้นผิดจังหวะโดยเฉพาะ atrial
fibrillation และอาจเกิด congestive heart failure ได้ในผู้ป่วยสูงอายุที่มีโรคหัวใจอยู่ก่อน
ในระบบประสาทและกล้ามเนื้อ
พบมีการทำงานมากขึ้นของ sympathetic
activity ทำให้เกิด tremor, hyperactivity, emotional
lability, anxiety, inability to concentrate และนอนไม่หลับ
ในระบบทางเดินอาหารพบมีการเพิ่มการเคลื่อนตัวของลำไส้
ทำให้หิวบ่อยขึ้นและกินมากขึ้น แต่น้ำหนักยังลด
Graves disease
Graves disease เป็นสาเหตุที่พบได้บ่อยสุดของ
hyperthyroidism ที่เกิดจากสาเหตุในต่อมไทรอยด์
พบได้บ่อยในช่วงอายุ 20-40 ปี พบในเพศหญิงมากกว่าเพศชาย (7:1) ปัจจัยทางพันธุกรรมเป็นสาเหตุของโรคนี้
การวินิจฉัยอาศัยลักษณะสำคัญทางคลินิก 3 อย่างต่อไปนี้
1.
hyperthyroidism
2.
infiltrative opthalmopathyทำให้ตาโปน (exophthalmos)
3.
localized infiltrative dermopathy
: pretibial myxedema ซึ่งพบได้น้อย
ปัจจุบันเป็นที่ยอมรับกันว่า Graves disease เป็นโรคออโตอิมมูน (autoimmune disorder)
เกิดจากการมี autoantibodies ต่อ TSH receptor,
thyroid peroxisomes และ thyroglobulin ในจำนวนนี้
autoantibodies ต่อ TSH receptor
ถือเป็นศูนย์กลางของกลไกการเกิดโรค
อาการและอาการแสดงของ Graves disease ได้แก่ ภาวะ hyperthyroidism, ต่อมไทรอยด์โตแบบทั่วไป(diffuse
goiter), ความผิดปกติที่ตา (opthalmopathy) และความผิดปกติที่ผิวหนัง (dermopathy : localized myxedema) อย่างไรก็ตามผู้ป่วยไม่จำเป็นต้องมีลักษณะดังกล่าวครบทุกราย
การที่มีภาวะ hyperthyroidism และมี diffuse goiter ในทางปฏิบัติสามารถให้การวินิจฉัยเบื้องต้นว่าเป็น diffuse goiter ได้ หรือในบางรายที่มีภาวะ hyperthyroidism
ร่วมกับมีอาการทางตา (opthalmopathy) โดยไม่มี diffuse
goiter ก็สามารถให้การวินิจฉัยได้เช่นกัน
Cretinism

Cretinism คือ hypothyroidism
ที่เกิดในเด็กทารกหรือเด็กเล็ก คำว่า cretin ได้มาจากคำว่า
chretienในภาษาฝรั่งเศสที่แปลว่า Christian หรือ Christ-like ใช้กับเด็กเหล่านี้เพราะปัญญาอ่อนเกินกว่าที่จะก่อบาปได้
ในอดีตโรคนี้เกิดในพื้นที่ขาดไอโอดีน แต่พบได้น้อยลงในปัจจุบัน
เนื่องจากมีการเสริมไอโอดีน
ลงในอาหาร
อาการแสดงของ Cretinism ได้แก่ ความผิดปกติของการเจริญเติบโตของกระดูกและสมอง ทำให้มีอาการปัญญาอ่อนอย่างมาก
ตัวเตี้ย ใบหน้าหยาบ ลิ้นคับปากและ umbilical hernia ความรุนแรงของอาการทางสมองเป็นผลโดยตรงจากการที่ขาดไทรอยด์ฮอร์โมนตั้งแต่อยู่ในครรภ์
โดยปกติแล้วฮอร์โมนของมารดารวมถึง T3 และ T4 จะผ่านรกและมีส่วนสำคัญอย่างยิ่งต่อการพัฒนาของสมองทารกในครรภ์ ถ้าขาดฮอร์โมนของมารดาก่อนที่ทารกจะมีการสร้างต่อมไทรอยด์ของตนเอง
ระดับความบกพร่องของสติปัญญาจะรุนแรงมาก
ในทางตรงข้ามถ้าระดับฮอร์โมนของมารดาต่ำลงหลังจากที่ทารกมีการสร้างต่อมไทรอยด์ของตนเองแล้ว
การเจริญเติบโตของสมองจะเป็นปกติ
Myxedema

Myxedema ใช้กับ hypothyroidism ที่เกิดในเด็กโตหรือผู้ใหญ่ อาการแสดงขึ้นกับอายุเริ่มต้นในขณะที่เป็นโรค
ในเด็กโตจะมีระดับอาการกึ่งกลางระหว่าง Cretinism ในเด็กเล็กและผู้ใหญ่ที่เป็น
hypothyroid ในผู้ใหญ่อาการจะค่อยเป็นค่อยไปและอาจใช้เวลาเป็นปีกว่าจะอยู่ในระดับที่ต้องสงสัยว่าเป็น
hypothyroidism
อาการของ hypothyroidism ในระยะแรกอาจดูคล้ายอาการซึมเศร้า
โดยมีการดำเนินกิจกรรมทางร่างกายและจิตใจช้าลง ผู้ป่วยจะเฉยชา ทนต่ออากาศหนาวไม่ได้
และมักพบว่ามีน้ำหนักเกิน หายใจถี่และออกกำลังกายได้น้อยลง
ผิวหนังของผู้ป่วยจะเย็นและซีดเนื่องจากเลือดไปเลี้ยงน้อยลง
การเคลื่อนไหวของลำไส้ลดลงทำให้มีอาการท้องผูก พบน้ำในช่องเยื่อหุ้มหัวใจได้บ่อย
เมื่อเป็นมากขึ้นหัวใจจะมีขนาดใหญ่ขึ้นและมีภาวะหัวใจวายตามมา
พาราไทรอยด์ฮอร์โมน
(parathyroid
hormone)

ต่อมพาราไทรอยด์มี 4
ต่อมอยู่ด้านหลังของต่อมไทรอยด์ ทำหน้าที่สังเคราะห์พาราไทรอยด์ฮอร์โมน (parathyroid
hormone, PTH หรือparathormone)
ซึ่งจำเป็นสำหรับการเพิ่มระดับแคลเซียมในเลือด
การสังเคราะห์และการหลั่ง PTH
ตัวกระตุ้นที่มีการหลั่งPTH
ที่สำคัญคือ ระดับ Ca²+ในเลือดที่ต่ำลง
ซึ่งหากลดต่ำกว่า 3.5 มก./ดล. จะกระตุ้นตัวรับCa²+ที่เยื่อหุ้ม chief cell ผ่าน G protein ทำให้ cAMPในเซลล์เพิ่มขึ้น ซึ่งจะลดระดับ Ca²+ ภายใน chief cell ทำให้เกิด exocytosis ของ PTH
PTH ออกฤทธิ์โดยการจับกับตัวรับที่เยื่อหุ้มเซลล์
กระตุ้นผ่าน adrenylatecyclaseเพิ่ม cAPMนอกจากนี้ PTH ยังกระตุ้นให้ Ca²+เข้าเซลล์โดยออกฤทธิ์ผ่านการเพิ่มของ phosphoinositideอวัยวะเป้าหมายสำคัญซึ่ง PTH ไปออกฤทธิ์โดยตรงได้แก่
กระดูกและไต และออกฤทธิ์โดยอ้อมต่อเซลล์ผนังทางเดินอาหารโดยผ่านวิตามินดี PTH กระตุ้นทั้งการสร้างและการสลายกระดูก
ในคนหรือสัตว์ที่ถูกตัดต่อมพาราไทรอยด์ออกหมด Ca²+
ในเลือดจะต่ำลง ขณะที่ PO4
¯
เพิ่มสูงขึ้นและเสียชีวิตภายในเวลาไม่กี่ชั่วโมงถ้าไม่ได้รับ PTH ทดแทน
ความผิดปกติของการหลั่ง PTH
PTH มากผิดปกติ (hyperparathyroidism) ทำให้ Ca²+ ในกระดูกน้อยลง (osteopenia) แต่ Ca²+ ในเลือดและปัสสาวะเพิ่มขึ้น (hypercalcemiaและ hypercalciuria) โดย hypercalciuriaอาจทำให้เกิดนิ่วCa²+ ในทางเดินปัสสาวะได้
PTH น้อยผิดปกติ (hypoparathyroidism) เกิด hypocalcemiaมีผลให้ excitability ของเซลล์ประสาทและกล้ามเนื้อเพิ่มขึ้น
โดยเฉพาะระบบประสาทส่วนปลายที่เลี้ยงกล้ามเนื้อ ถ้า Ca²+
ในพลาสมาต่ำกว่า 6 มก./ดล. จะเกิด hypocalcemiatetanyได้ ถ้า Ca²+
ต่ำมากอาจชักทั้งตัวและเสียชีวิตอย่างรวดเร็ว
วิตามินดีมีความสำคัญต่อการควบคุม Ca²+ และ PO4
¯ ในเลือดให้คงที่โดยเพิ่มการดูดซึม
Ca²+ และ PO4
¯
จากอาหาร และจำเป็นสำหรับการเจริญของกระดูก ถ้าได้รับ Ca²+,PO4
¯และวิตามินดีจากอาหารน้อยลง
ทำให้ระดับ Ca²+ และ PO4
¯
ในเลือดต่ำลงจะกระตุ้น PTH
ให้หลั่งมากขึ้น
โรคที่พบในความผิดปกติของต่อมพาราไทรอยด์
Hyperparathyroidism
Hyperparathyroidism
แบ่งเป็น สองประเภทหลักคือ primary และ secondary ส่วน tertiary พบได้น้อย primary
hyperparathyroidism หมายถึง ภาวะที่ต่อมสร้าง PTH ออกมามากด้วยตัวต่อมเอง secondary และ tertiary
เป็นปรากฏการณ์ที่เกิดขึ้นในผู้ป่วยโรคไตเรื้อรัง
primary hyperparathyroidism เป็นหนึ่งในภาวะความผิดปกติของต่อมไร้ท่อที่พบบ่อยที่สุด
และเป็นสาเหตุสำคัญของ hypercalcemiaอาการและอาการแสดงเป็นผลร่วมกันจากการหลั่ง
PTH เพิ่มขึ้นและ hypercalcemiaโดย primary hyperparathyroidism
สัมพันธ์กับกลุ่มอาการดังต่อไปนี้ “painful bones, renal stones, abdominal
groans, and psycic moans”
- Bone disease ได้แก่
อาการปวดกระดูกเนื่องจากกระดูกที่อ่อนแอจาก osteoporosis หรือ
osteitisfibrosacysticaหัก
- Nephrolithiasis เกิดใน 20
%ของผู้ป่วยรายใหม่โดยมีอาการปวดและอาการของ obstructive
uropathyพบ chronic renal insufficiency และความผิดปกติของการทำงานของไตหลายอย่างรวมถึง
polyuria และ polydipsia
- Gastrointestinal disturbances ได้แก่ ท้องผูก คลื่นไส้ แผลในกระเพราะอาหาร ตับอ่อนอักเสบ
ละนิ่วในถุงน้ำดี
- Central nervous system alteration ได้แก่ อาการซึมเศร้า ง่วงซึมและชัก
- Neuromuscular abnormalities ได้แก่ อาการอ่อนแรงและอ่อนเพลีย
- Cardiac manifestation ได้แก่
aortic หรือ mitral valve calcifications
Hypoparathyroidism
Hypoparathyroidism
พบได้น้อยกว่า Hyperparathyroidism อาการที่พบส่วนใหญ่เกิดจากภาวะ
hypocalcemiaและอาการสำคัญของภาวะ hypocalcemia คือ tetanyซึ่งมีลักษณะสำคัญคือ neuromuscular
irritability ทำให้มีอาการได้ตั้งแต่ชารอบริมฝีปาก ไปจนถึง laryngospasm
และ generalized seizures ที่เป็นอันตรายต่อชีวิต
การตรวจร่างกายที่พบได้บ่อยในผู้ป่วยที่มี neuromuscular irritability ได้แก่ Chovstek sign และ Trousseau sign โดย Chovstek sign
สามารถตรวจพบได้ในผู้ป่วยที่มีอาการน้อย โดยการเคาะที่ facial nerve ซึ่งจะทำให้มีการหดตัวของกล้ามเนื้อของตา
ปาก หรือจมูก ส่วน Trousseau sign
ทำได้โดยการกดการไหลเวียนที่แขนและมือโดยใช้เครื่องวัดความดันรัดไว้และปล่อยลมเข้าไปประมาณ
2-3 นาที ทำให้เกิดมือจีบ
ซึ่งจะหายไปเมื่อคลายเครื่องวัดความดันออก
ต่อมหมวกไต
(adrenal
gland)

ต่อมหมวกไตได้ชื่อนี้เนื่องจากวางอยู่บนไตทั้งสองข้าง
แต่ละต่อมประกอบด้วยชั้นนอก (cortex) หรือเรียกว่า
ต่อมหมวกไตส่วนเปลือก (adrenal cortex) สังเคราะห์ steroids
ที่แตกต่างกันสามชนิดได้แก่
1) glucocorticoids 2)
mineralocorticoids 3) sex steroids (estrogens
และ androgens) และชั้นใน (medulla) หรือเรียกว่า ต่อมหมวกไตส่วนใน (adrenal medulla)
ประกอบด้วย chromaffin cells หลั่งและสังเคราะห์ catecholaminesซึ่งประมาณร้อยละ 80 เป็น epinephrine (adrenaline) และร้อยะ 20 เป็น
norepinephrine (noradrenaline)
ฮอร์โมนต่อมหมวกไตส่วนเปลือก(adrenocortical
hormones)
ต่อมหมวกไตส่วนนอกแบ่งได้เป็น
3 ส่วน ส่วนนอกบางสุดอยู่ติดแคปซูล (zonaglomerulosa) ส่วนกลาง (zonafasciculata) หนาที่สุด
และส่วนในสุด (zonareticularis) อยู่ชิด medulla กลไกควบคุมการสร้างและการหลั่งฮอร์โมนนี้แตกต่างกัน ส่วนfasciculate และreticularis อยู่ภายใต้การควบคุมของ ACTH
จากต่อมใต้สมอง แต่ส่วนglomerulosa
ถูกควบคุมโดยฮอร์โมนของไต ได้แก่ renin และ angiotensin
แบ่งฮอร์โมนต่อมหมวกไตส่วนปลือกตามการออกฤทธิ์ได้ 3 กลุ่มคือ
1. mineralocorticoid สร้างมากที่สุดโดยเซลล์ชั้นglomerulosa ทำหน้าที่รักษาปริมาตรเลือดmineralocorticoid
ที่สำคัญที่สุดคือ aldosterone ทำหน้าที่ควบคุมดุลน้ำและเกลือแร่
ออกฤทธิ์ที่เซลล์ของหลอดไตส่วน distal tubule และ collecting
duct ขับ Na+ ภายในเซลล์ออกสู่สารน้ำนอกเซลล์และเข้าสู่เลือดมากขึ้น
Na+ ในเซลล์ลดลง ขณะเดียวกัน aldosterone กระตุ้น Na+channel ที่ผนังเซลล์หลอดไตด้านติด lumen
ให้เปิดมากขึ้น Na+ และน้ำใน lumen ถูกดูดกลับเข้าสู่เซลล์เพิ่มขึ้น และเซลล์ก็ขับ K+ และ
H+ ออกมาใน lumen เพื่อแลกกับNa+ จึงทำให้เลือดเป็นด่างเพิ่มขึ้น ผลโดยรวมของ aldosterone ทำให้Na+ และน้ำในเลือดเพิ่มขึ้น
ความดันเลือดแดงและ cardiac output จึงเพิ่มตาม
และป้องกันไม่ให้ร่างกายมีK+ ในเลือดสูง (hyperkalemia)
aldosterone มากผิดปกติอาจเป็นชนิด
primary (Conn’s syndrome) เช่น
มีเนื้องอกต่อมหมวกไตทำให้เกิดการคั่งของ Na+ และน้ำ
มีผลให้น้ำหนักตัวเพิ่ม ความดันเลือดสูง K+ ในพลาสมาต่ำลง (hypokalemia) เลือดเป็นด่างมากขึ้นจากการเสีย H+ ออกทางปัสสาวะ
(metabolic alkalosis)
ภาวะขาด aldosterone
มักเกิดร่วมกับการขาด cortisol (Addison’s disease) ร่างกายสูญเสีย Na+ และน้ำทางปัสสาวะมาขึ้น K+ ในพลาสมาสูงและเลือดเป็นกรดมากขึ้น (metabolic acidosis) ปริมาตรเลือดลดลง (hypovolemia)
2. Glucocorticoid cortisol เป็น Glucocorticoid ที่มีความสำคัญต่อการเจริญและพัฒนาการของทารกในครรภ์
cortisol เพิ่มการสร้างกลูโคสและไกลโคเจนภายในตับและเร่งให้มีการปล่อยกลูโคสจากตับออกสู่เลือดมากขึ้น
การมี cortisol ระดับปกติมีความจำเป็นอย่างยิ่งต่อการผลิตกลูโคส
ทำให้เซลล์ของร่างกายโดยเฉพาะเซลล์ของสมองมีกลูโคสใช้อย่างเพียงพอในระหว่างอดอาหาร
cortisol
มีฤทธิ์ต่อกล้ามเนื้อ
กล้ามเนื้อโครงสร้างและกล้ามเนื้อหัวใจจะหดตัวและทำงานปกติต้องอาศัย cortisolการรักษาระดับความดันเลือดให้ปกติต้องอาศัย cortisol
เนื่องจากช่วยให้หัวใจหดตัวได้แรง ถ้าขาด cortisol
มีผลให้เกิดความดันเลือดต่ำขณะยืน (postural hypotension)
ได้ง่าย
cortisol ในระดับปกติไม่มีฤทธิ์ยับยั้งการอักเสบและการตอบสนองทางระบบภูมิคุ้มกัน
ในทางคลินิกใช้ cortisol
ขนาดสูงกว่าปกติเป็นยายับยั้งการอักเสบ cortisol
ทำให้ไขกระดูกปล่อยเซลล์เม็ดเลือดขาวเข้ามาในเลือดมากขึ้น
แต่เซลล์ถูกกดให้ทำงานน้อยลง เซลล์และพลาสมาผ่านออกจากหลอดเลือดไปสู่บริเวณที่มีการทำลายหรือมีการอักเสบของเนื้อเยื่อได้น้อยลง
อาการบวมจะลดลง
cortisol ลดจำนวน T-lymphocyte
ในกระแสเลือด มีผลให้ B-lymphocyte ที่สร้างภูมิคุ้มกันชนิด
hormone antibody ลดตามไปด้วย
ทำให้ภูมิคุ้มกันของร่างกายลดลงทำให้ cortisol
ถูกใช้เป็นยายับยั้งปฏิกิริยาภูมิแพ้ที่รุนแรง (anti-allergy)
เช่น โรคหอบหืด (asthma) และป้องกันการเกิด graft
rejection ในผู้ป่วยที่มีการปลูกถ่ายหรือเปลี่ยนอวัยวะ
ภาวะขาด cortisol เพียงลำพังพบได้น้อย
มักพบร่วมกับการขาด mineralocorticoidต่อมหมวกไตทำงานน้อยอาจเป็นชนิด
primary (Addison’sdisease) การมี cortisolมากผิดปกติ (Cushing’s syndrome) มักพบเป็นชนิด secondary
เนื่องจากมี ACTH เพิ่มขึ้น สำหรับชนิด primary ที่ต่อมหมวกไตผลิต cortisol มากเองพบไม่บ่อยนัก
แต่ผลที่เกิดขึ้นจะคล้ายกัน
3. adrenal sex hormone ACTH ควบคุมการสังเคราะห์ androgen ภายในต่อมหมวกไต
ฮอร์โมนเพศจากต่อมหมวกไตเพิ่มสูงเมื่อเด็กอายุ 7-9 ปี
สูงสุดประมาณอายุ 20 ปี และลดลงหลังอายุ 50 ปี ในคนเชื่อว่ามีฤทธิ์ทำให้ความต้องการทางเพศของชายและหญิงเพิ่ม
กระตุ้นการเจริญของ pubic hair และ axillary hair ในเพศหญิง
ฮอร์โมนต่อมหมวกไตส่วนใน
(adrenal
medullary hormone)
ต่อมหมวกไตส่วนในเป็นแหล่งผลิตของ catecholamines(epinephrine, norepinephrine) ในร่างกาย norepinephrine ทำหน้าที่เป็น local neurotransmitterสื่อระหว่างประสาทซิมพาเทติกกับเซลล์เป้าหมาย
มีจำนวนเล็กน้อยที่จะเข้าสู่กระแสเลือด epinephrine (adrenaline) จะหลั่งเข้าสู่กระแสเลือดซึ่งทำปฏิกิริยากับ adrenergic และ
adrenergicreceptors
ในเซลล์หลายชนิด เกี่ยวข้องกับ systemic action of
epinephrine เช่น
เพิ่มความแรงและความเร็วของการบีบตัวของกล้ามเนื้อหัวใจ
และทำให้เกิดหลอดเลือดหดตัวหลายบริเวณ epinephrineมีความสำคัญต่อการเคลื่อนย้ายพลังงานอาหารในร่างกายโดยทำงานเสริมกับไทรอยด์ฮอร์โมนและ
glucocorticoid เพิ่มกลูโคสและกรดไขมันอิสระในเลือดเพื่อใช้เป็นพลังงานแก่เซลล์ทำให้ระดับน้ำตาลในเลือดสูงขึ้น
นับเป็น diabetogenic hormone อีกชนิดหนึ่ง
ผลของ norepinephrine และ epinephrine
ต่อหัวใจและหลอดเลือดอาจเสริมกัน ตรงข้ามกันหรือ
บางครั้งชนิดใดชนิดหนึ่งไม่ออกฤทธิ์ ฤทธิ์ผ่านตัวรับ
ของ epinephrine มีผลเพิ่มอัตราเต้นและแรงหดตัวของหัวใจ cardiac output จึงเพิ่มขึ้น ขณะเดียวกันจะทำให้หลอดเลือดแดงของกล้ามเนื้อขยายขนาดขึ้น (vasodilation)
catecholamine
จากต่อมหมวกไตไม่สามารถผ่าน blood-brain barrier เข้าไปมีผลต่อสมองโดยตรงได้
ผลต่อระบบประสาทที่พบอาจเป็นผลทางอ้อมจากฤทธิ์ต่อหัวใจและหลอดเลือด
หรือจากสารที่เพิ่มขึ้นในเลือดและผ่านไปยังสมอง พบว่าทั้ง epinephrine และ norepinephrineทำให้เกิดความตื่นตัว ม่านตาขยาย
catecholamine มากผิดปกติอาจเกิดได้ทั้งเฉียบพลันและเรื้อรัง
อาการที่พบเกิดเนื่องมาจากหัวใจ หลอดเลือด สมองและระบบประสาทถูกกระตุ้น
ความดันเลือดสูงรวดเร็ว หัวใจอาจเต้นช้าลงหรือเร็วขึ้นผิวหนังซีด เหงื่อออก
ตัวเย็น ปวดศีรษะ ในระยะต้นๆอาการมักเกิดชั่วขณะ ในระยะหลัง catecholamineที่สูงต่อเนื่องเป็นเวลานานทำให้เมแทบอลิซึมสูง น้ำหนักตัวลด
ความดันเลือดสูงตลอดเวลา แต่มี postural hypotentionได้
โรคที่พบในความผิดปกติของต่อมหมวกไต
Cushing’s syndrome

ความผิดปกตินี้เกิดจากภาวะใดก็ตามที่ทำให้ระดับของ
glucocorticoids เพิ่มขึ้น ซึ่งมีที่มาได้สี่อย่าง
สาเหตุที่พบบ่อยที่สุดของ Cushing’s syndrome คือ การได้รับ glucocorticoids จากภายนอก (administration of exogenous glucocorticoids) สาเหตุที่เหลืออีกสามประการอาจเรียกรวมกันได้ว่า เป็นสาเหตุจากภายใน (endogenous
Cushing’s syndrome) ซึ่งได้แก่
- Primary hypothalamic-pituitary diseases
associated with hypersecretion of ACTH
- Hypersecretion of cortisol by an
adrenal adenoma, carcinoma or nodular hyperplasia
- The secretion of ectopic ACTH by a
non-endocrine neoplasm
Primary hypersecretion of ACTH เป็นสาเหตุ 70-80% ของผู้ป่วย endogenous Cushing’s
syndrome
เพื่อเป็นการให้เกียรติกับประสาทศัลยแพทย์คนแรกที่ได้อธิบายกลุ่มอาการนี้ที่สัมพันธ์กับรอยโรคในต่อม
ใต้สมอง จึงเรียกว่า Cushing’s syndrome
ความผิดปกตินี้พบในเพศหญิงมากกว่าเพศชาย และมักพบในช่วงอายุ 20-30 ปี
Primary adrenal neoplasmasเช่น
adrenal adenoma และ carcinoma และ
primary cortical hyperplasia เป็นสาเหตุ 10-20% ของผู้ป่วย endogenous Cushing’s syndrome
เกิดเนื่องจากต่อมหมวกไตทำงานเองโดยอัตโนมัติ คุณสมบัติของ adrenal
Cushing’s syndrome คือระดับ cortisol
ในเลือดสูงขึ้นและระดับ ACTH ต่ำลง
ฮอร์โมนของตับอ่อน

นอกจากตับอ่อนจะผลิตและหลั่งน้ำย่อยเอนไซม์สูงสู่ลำไส้เล็ก
ซึ่งเป็นบทบาทสำคัญในระบบการย่อยอาหารแล้ว
ยังรับหน้าที่เป็นต่อมไร้ท่ออีกทางหนึ่งโดยสร้างฮอร์โมนสองชนิดที่มีส่วนในการเผาผลาญคาร์โบไฮเดรตและควบคุมระดับกลูโคสในเลือด
ฮอร์โมนชนิดแรกคือ อินซูลิน (insulin) ซึ่งทำให้กลูโคสจากเลือดผ่านเข้าสู่ภายในเซลล์ได้มากขึ้นเพื่อใช้เป็นสารอาหารและเป็นแหล่งพลังงานหลัก
การทำงานของอินซูลินส่งผลให้ระดับกลูโคสในเลือดต่ำ (hypoglycemia) เนื่องจากความเข้มข้นของกลูโคสในเลือดลดลง
ฮอร์โมนจากตับอ่อนอีกชนิดหนึ่งคือ กลูคากอน (glucagon) ซึ่งทำงานตรงข้ามกับอินซูลินคือทำให้ระดับกลูโคสในเลือดสูง
(hyperglycemia)
เนื่องจากช่วยเร่งการแตกตัวของไกลโคเจนที่เก็บไว้ในเซลล์
และทำให้กลูโคสผ่านเข้าสู่เลือดได้มากขึ้น
1.อินซูลิน (insulin)
ปัจจัยที่เพิ่มการหลั่งอินซูลินได้แก่
กรดอะมิโน กรดไขมัน และสารคีโทนในเลือด การกระตุ้นประสาทซิมพาเทติกผ่านตัวรับ
–adrenergic และประสาทเวกัส
รวมทั้งกลูคากอนและฮอร์โมนของทางเดินอาหารหลายชนิด
ซึ่งอาจเป็นสาเหตุให้การรับประทานเพิ่มระดับน้ำตาลในเลือดได้สูงกว่าการให้น้ำตาลทางหลอดเลือด
ฮอร์โมนอื่นๆ เช่นACTH, TSH, thyroid hormone, GH, estrogen, progesterone และ human placental lactogenที่ระดับสูงกว่าปกติมีฤทธิ์เพิ่มการหลั่งอินซูลินเช่นกัน
ในขณะเดียวกันอินซูลินที่สูงยังทำให้เซลล์เป้าหมายตอบสนองต่ออินซูลินได้น้อยลง
เกิดภาวะดื้อต่ออินซูลิน (insulin resistance)
มีผลให้กลูโคสยิ่งเพิ่มสูงมากขึ้น คนอ้วนที่มีระดับน้ำตาลในเลือดสูงตอดเวลาเกิด insulin
resistance เช่นกัน
การออกกำลังกายเป็นประจำสามารถแก้ไขภาวะดื้อต่ออินซูลินได้
ปัจจัยที่ลดการหลั่งอินซูลินได้แก่ การกระตุ้นประสาทซิมพาเทติกผ่านตัวรับ
–adrenergic รวมทั้ง somatostatinของตับอ่อนและไฮโปทาลามัส
การทดสอบความสามารถของเซลล์ B
ในการสร้างอินซูลินอาจทำโดยการวัดระดับอินซูลิน หรือ C-peptide ในเลือด นอกจากนี้การทดสอบความทนกลูโคส (glucose tolerance test,
GTT) เป็นวิธีสำคัญอีกประการหนึ่งที่ใช้บอกสมรรถภาพของเซลล์ B
คนปกติภายหลังการอดอาหารนานกว่า 8-10 ชั่วโมง
ระดับน้ำตาลในเลือด (fasting blood glucose) ควรต่ำกว่า 115 มก./ดล. ถ้าให้กลูโคสโดยวิธีรับประทาน (oral glucose tolerance test,
OGTT)หรือฉีดเข้าหลอดเลือดดำ (intravenous glucose tolerance
test, IVGTT)ระดับอินซูลินในเลือดจะเพิ่มขึ้นตามการเพิ่มของกลูโคส
มีผลทำให้กลูโคสลดต่ำลง ในรายที่เซลล์ B ทำงานปกติกลูโคสในเลือดจะลดกลับมามีค่าต่ำกว่า
140 มก./ดล. ที่ 2
ชั่วโมงหลังจากดื่มสารละลายกลูโคส แต่ในรายที่เซลล์ B
สร้างอินซูลินไม่ได้หรือไม่พอกับความต้องการของร่างกาย ระดับน้ำตาลที่ 2 ชั่วโมงจะสูงกว่า 200 มก./ดล. ระดับน้ำตาลที่ 2 ชั่วโมงที่มีค่าระหว่าง 140-200 มก./ดล. เรียกว่า
มีความผิดปกติของการทนกลูโคส (impaired GTT, IGT)
เป็นภาวะก่อนเป็นเบาหวาน (prediabetes)
ความผิดปกติของการหลั่งอินซูลิน
อินซูลินมากผิดปกติสาเหตุที่พบบ่อยคือ
ขนาดของอินซูลินที่ให้แก่ผู้ป่วยเบาหวานมากเกินไป
นอกจากนี้อาจเกิดจากโรคที่พบได้ยาก ได้แก่ เนื้องอกของตับอ่อนที่สร้างอินซูลิน
การเพิ่มสูงของอินซูลินมีผลทำให้ระดับน้ำตาลในเลือดต่ำกว่าปกติ
เมื่อระดับน้ำตาลในเลือดต่ำกว่า 50 มก./ดล. (hypoglycemia) จะทำให้เซลล์สมองขาดสารอาหาร
ร่างกายจะตอบสนองโดยการเพิ่มการทำงานของระบบประสาทซิมพาเทติกเพื่อเพิ่มระดับน้ำตาลในเลือด
ทำให้เกิดอาการต่างๆได้แก่
1.
neuroglycopenisเช่น
hunger, dizziness or confusion, lateralizing neurological signs, coma
2.
catecholamine เช่น anxiety,
fear, agitation, sweating, pallor, tachycardia, palpitation
การขาดอินซูลินทำให้เกิดโรคเบาหวาน (diabetes
mellitus) พบได้ 2 ชนิด ชนิดแรกเรียกว่า type I diabetes mellitus หรือ insulin-dependent diabetes mellitus (IDDM) ผู้ป่วยจำเป็นต้องได้รับอินซูลินทดแทนจากภายนอกตลอดชีวิตเพราะตับอ่อนถูกทำลายโดยไม่ทราบสาเหตุที่แน่นอนทำให้ไม่มีการสังเคราะห์หรือสังเคราะห์อินซูลินได้น้อยมาก
มักพบในคนอายุน้อย โรคเบาหวานชนิดสอง เรียกว่า type II diabetes mellitus หรือ
non-insulin-dependent diabetes mellitus (NIDDM)เนื่องจากผู้ป่วยยังสามารถสังเคราะห์อินซูลินได้
สาเหตุการเกิดโรคนี้แบ่งได้ 2 ส่วน
สาเหตุแรกคือผิดปกติที่การหลั่ง เช่น หลั่งน้อยลงเนื่องจากเซลล์ Bไม่ตอบสนองหรือตอบสนองต่อกลูโคสน้อยลง สาเหตุที่สองคือ insulin
resistance เกิดจากอินซูลินหลั่งออกมาได้แต่ไม่สามารถออกฤทธิ์ต่อเซลล์ของร่างกายได้ตามปกติ
NIDDM พบในผู้สูงอายุร่วมกับปัจจัยเสี่ยงอื่นๆ เช่น
ความอ้วนและพันธุกรรม
การขาดอินซูลินทำให้เซลล์ทั่วไปไม่สามารถใช้กลูโคสเป็นพลังงานได้
ต้องเปลี่ยนมาใช้ไขมันและโปรตีนแทน ไกลโคเจนในตับสลายเป็นกลูโคสและปล่อยออกสู่กระแสเลือดได้มากขึ้น
triglyceride
ถูกสลายทำให้กรดไขมันอิสระและ glycerol
ในเลือดมากขึ้นด้วย ตับสร้างคีโทนและปล่อยออกสู่กระแสเลือดโดยคีโทนจะถูกนำไปใช้เป็นพลังงานที่กล้ามเนื้อและสมอง
คีโทนมีสภาวะเป็นกรดเลือดจึงมีความเป็นกรดสูง (acidosis) มีการสูญเสียไขมันและโปรตีนสะสมของร่างกาย
น้ำหนักลด พบน้ำตาลในปัสสาวะ (glycouria)
ทำให้เสียน้ำออกจากร่างกายทางปัสสาวะมากด้วย (polyuria)
ทำให้ผู้ป่วยเบาหวานกระหายน้ำมาก ดื่มน้ำมาก โรคแทรกซ้อนจากการมีน้ำตาลในเลือดสูงเป็นเวลานานเกิดได้ทั้งในระยะเฉียบพลันและระยะยาว
ภาวะเฉียบพลัน เช่น diabetic ketoacidosis (DKA) และ hyperosmolar coma ภาวะแทรกซ้อนระยะยาวที่พบมากคือเกิดการเปลี่ยนแปลงของหลอดเลือดแดงขนาดเล็กที่จอตา
(retina) ไต เส้นเลือดที่เลี้ยงเส้นประสาท สมอง และกล้ามเนื้อหัวใจ
(coronary artery) เป็นต้น ทำให้เกิด diabetic
retinopathy, nephopathy, neuropathy, เส้นเลือดสมองอุดตันและ ischemic
heart disease ตามลำดับ
และยังอาจเกิดการเปลี่ยนแปลงของหลอดเลือดแดงขนาดใหญ่ที่ทำให้เกิดความดันเลือดสูงได้
2. กลูคากอน (glucagon)
กลูคากอนมีฤทธิ์ส่วนใหญ่ตรงข้ามกับฤทธิ์ของอินซูลินคือ
กระตุ้นให้มีการดึงพลังงานจากสารอาหารออกมาใช้มากกว่าเก็บสะสมไว้โดยเฉพาะที่ตับ
ทำให้ระดับน้ำตาลที่ปล่อยจากตับเพิ่มขึ้นจากการสลายไกลโคเจนและการสังเคราะห์น้ำตาลขึ้นใหม่
กลูคากอนมากผิดปกติอาจเกิดจากมะเร็งของตับอ่อน
ความผิดปกติของเมแทบอลิซึมของสารอาหารในร่างกาย ผู้ที่มีกลูคากอนมากจะเกิดเหมือนกับที่พบในผู้ที่ขาดอินซูลิน
ได้แก่ ระดับน้ำตาลในเลือดสูง ซึ่งอาจมีผลกระตุ้นเซลล์ B
ให้ผลิตอินซูลินมากจนเกิดการล้าและผลิตไม่พอ กลายเป็นเบาหวานตามมาได้
ผู้ป่วยเบาหวานซึ่งขาดอินซูลิน
ทำให้กลูโคสเข้าเซลล์น้อยลงมีผลต่อการกระตุ้นการสังเคราะห์และการหลั่งกลูคากอน
ดังนั้นผู้ป่วยเบาหวานบางรายอาจมีระดับกลูคากอนเพิ่มสูงกว่าปกติร่วมกับการขาดอินซูลิน
ทำให้ความผิดปกติของเมแทบอลิซึมรุนแรงมากขึ้นอีก โดยเฉพาะจะมีการสร้างคีโทนเพิ่มมากขึ้น
โอกาสเกิดภาวะแทรกซ้อนจาก ketoacidosis
จึงมากขึ้นด้วย
โรคที่พบในความผิดปกติของตับอ่อน
Diabetes mellitus (เบาหวาน)
เบาหวานเป็นกลุ่มของ metabolic
disorders ซึ่งมีจุดกำเนิดร่วมกันคือน้ำตาลในเลือดสูง (hyperglycemia) ภาวะน้ำตาลในเลือดสูงของผู้ป่วยเบาหวานเกิดจากความผิดปกติในการหลั่งอินซูลิน
การทำงานของอินซูลิน หรือที่พบบ่อยคือเป็นผลจากทั้งสองอย่าง
การที่มีน้ำตาลในเลือดสูงเป็นระยะเวลานาน
และการควบคุมระบบการเผาผลาญที่เปลี่ยนแปลงไป
อาจสัมพันธ์กับความเสียหายในหลายอวัยวะตามมา โดยเฉพาะใน ไต ตา เส้นประสาท
และเส้นเลือด เบาหวานเป็นสาเหตุหลักของไตวายระยะสุดท้าย การตาบอดในผู้ใหญ่
และการตัดขาที่ไม่ได้เกิดจากอุบัติเหตุ
Type 1 diabetes เกิดจากการขาดอินซูลินเพียงอย่างเดียวเนื่องจากมีการทำลายของ
cell
ซึ่งคิดเป็น 10% ของผู้ป่วยทั้งหมด
Type 2 diabetes
เกิดจากผลร่วมกันระหว่าง peripheral resistant ต่อการทำงานของอินซูลิน
และ
cell ไม่สามารถตอบสนองได้อย่างเพียงพอ ซึ่งคิดเป็น 80-90% ของผู้ป่วยทั้งหมด
ฮอร์โมนต่อมไพเนียล
(pineal
hormone)
ต่อมไพเนียลอยู่ตรงกลางติดกับบริเวณด้านหลังของ
third
ventricle ในสมอง ทำหน้าที่สังเคราะห์ serotonin จากกรดอะมิโน tryptophan ซึ่งถูกเปลี่ยนเป็นเมลาโทนิน
(melatonin) แล้วขับออกสู่เลือดหรือน้ำไขสันหลัง
การสังเคราะห์เมลาโทนินถูกควบคุมด้วยการเปลี่ยนแปลงในรอบวันของแสง โดยแสงยับยั้งการสร้างในขณะที่ความมืดกระตุ้นการสร้างเมลาโทนิน
ดังนั้นต่อมไพเนียลจึงถูกเรียกว่า third eye
เมลาโทนินมีผลต่อระบบที่เกี่ยวข้องกับแสงและจังหวะรอบวัน
เช่น ระบบสืบพันธ์ รอบการนอนหลับและการตื่น เป็นต้น
เด็กที่มีความผิดปกติของต่อมไพเนียลจะเป็นหนุ่มสาวเร็วกว่าปกติ (precocious puberty) ฤทธิ์ต่อรอบการนอนและการตื่น
พบว่าเมื่อให้เมลาโทนินขนาดสูงสามารถรักษาผู้ป่วยนอนไม่หลับได้
และป้องกันอาการผิดปกติอันเกิดจากการเปลี่ยนแปลงเวลาหลังจากเดินทางไกลๆโดยเครื่องบิน
(jet lag)
สรุป ระบบต่อมไร้ท่อเป็นระบบที่ซับซ้อนและสัมพันธ์กับระบบต่างๆของร่างกายแทบทุกระบบ
โดยเฉพาะระบบประสาทและระบบไหลเวียนเลือด
เกี่ยวข้องกับกระบวนการเมแทบอลิซึมของร่างกาย สารที่หลั่งออกมาเรียกว่าฮอร์โมน
ซึ่งมีผลต่อเนื้อเยื่อเป้าหมาย (target cell) ในร่างกาย
ถ้ามีความผิดปกติของการหลั่งฮอร์โมน เช่น หลั่งมากเกินไป หรือหลั่งน้อยเกินไป
จะส่งผลกระทบกับเนื้อเยื่อเป้าหมาย ทำให้เกิดโรคต่างๆตามมา
และยังส่งผลถึงกระบวนการเจริญเติบโตของร่างกาย ตามการออกฤทธิ์ของฮอร์โมนแต่ละชนิด
ดีมากข้อมูลละเอียดมาก ช่วยในการติวสอบได้ดีมาก
ตอบลบ